무너지는 바이오 스타트업의 꿈…IPO까지 평균 10년
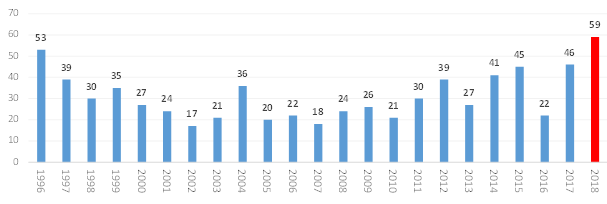
메디칼타임즈=황병우 기자바이오산업의 토대가 되는 스타트업들이 한없이 보릿고개를 겪으면서 기업 공개, 즉 IPO의 꿈이 점점 더 멀어져가고 있다.매출 성과가 나온다 해도 평균 영업이익과 순이익이 마이너스 지표를 보이고 있기 때문. 이로 인해 주요 투자자금 확보 방안 중 하나인 기업공개(IPO)도 평균 10년 이상이 소요되고 있다는 점에서 이 기간을 버틸 수 있는 방안이 필요하다는 목소리가 나오고 있다.생명공학정책연구센터는 지난달 말 '2020년 기준 국내 바이오 중소벤처기업 현황 통계'를 발표했다.생명공학정책연구센터는 4일 '2020년 기준 국내 바이오 중소벤처기업 현황 통계'를 내고 국내 바이오 분야의 중소·벤처기업의 현황을 분석했다.보고서는 1992년부터 2020년까지 조사대상기업 3384개 중 폐업기업 603개를 제외한 2781개 생존기업 및 휴업기업을 대상으로 진행됐다.먼저 바이오 중소벤처기업의 숫자 변동 추이를 보면 2000년 바이오 벤처기업 붐 이후 최근까지 바이오 기업에 대한 관심이 높아지면서 창업은 계속해서 증가하고 있다. 최근 5년 간 평균 창업기업 수는 약 401개로 2000년대 약 148개, 2010년대 약 312개와 비교하면 각각 2.7배와 1.3배 높아졌다. 이 기간 중 가장 많은 수의 기업이 창업된 시기는 2016년의 546개였다.2020년 기준 국내 바이오 중소벤처기업 현황 통계 일부발췌분석 기업을 분야별로 분류했을 때는 의약품(613개)과 진단의료기기(280개)를 포함한 레드바이오가 893개로 가장 많았으며 ▲그린바이오 805개 ▲플랫폼바이오 545개 ▲화이트바이오 538개 순으로 분포했다.의약품과 진단의료기기가 포함된 레드바이오를 중심으로 보고서를 살펴보면 기업공개(IPO)를 실시한 기업은 2020년 기준 전체 205개 기업으로 이중 레드바이오 영역은 의약품 79개, 진단의료기기 26개 등 총 105개였다. 이를 세부항목별로 봤을 땐 ▲유가증권 3개 ▲코넥스 17개 ▲코스닥 85개였다.중소벤처바이오기업 IPO 까지 평균 10년 소요…의약품 분야 평균 9.1년또한 기업공개 경험이 있는 205개 기업의 기업공개까지 걸리는 기간은 평균 10년이 소요됐으며 의약품 분야는 평균 9.1년, 진단의료기기 분야는 평균 10.3년이 걸리는 것으로 조사됐다.이와 함께 바이오 중소벤처기업의 경영성과 현황을 살펴봤을 때 평균 매출액은 의약품 분야 기업이 88.1억원으로 가장 높았으며 ▲식품 73.5억원 ▲진단의료기기 69.1억원 ▲화학63.6억원 순으로 나타났다.2020년 기준 국내 바이오 중소벤처기업 현황 통계 일부발췌다만 영업이익의 경우 의약품 분야가 평균 –13.6억원으로 가장 낮은 영업이익을 보였으며, 매출액 대비 영업이익률은 –15.4%를 기록했다. 평균 순이익역시 –23억원이었다.해당 지표가 각 분야별 기업의 영업이익 및 순이익 합계를 영업이익과 순이익이 발생한 기업수로 나눴다는 점을 고려했을 때 대다수 기업이 매출 면에서 플러스(+)지표를 기록하지 못했다는 것으로 해석이 가능하다.이러한 수치는 꾸준히 지적받고 있는 한국거래소 상장폐지 요건 완화와 함께 주의를 기울여야 할 부분으로 보인다.지난해 한국거래소는 상장사 퇴출 제도 합리화를 위한 상장 규정 개정을 예고한 바 있다. 상장폐지에 실질심사 전환을 실시했지만 여전히 상장 후 5년 간 연 매출 30억원 적용 유예 이후에는 매출이 중요 지표가 되는 만큼 구체적 수익 창출 방안이 있어야 하기 때문이다.이와 관련해 벤처캐피탈 관계자는 "신약 개발하는 기업의 경우 파이프라인이 망가져도 회사가 버틸 체력이 있어야 한다는 의미다"며 "상장폐지요건 완화로 바이오사의 숨통이 트일 수는 있겠지만 궁극적으로 연 매출이라는 숙제가 완전히 해결된 것은 아니다"고 밝혔다.의약품 분야 연구개발비 평균 15.6억원…매출액 대비 17.7% 투자아울러 보고서에서 바이오 중소벤처기업에서 가장 중요한 요소인 연구개발비의 평균은 의약품 분야가 15.6억원으로 가장 높았으며, 진단의료기기분야는 평균 6.2억원이었다.이를 매출액 대비 연구개발비로 전환해 살펴보면 의약품 분야가 17.7%로 가장 높았고 진단의료기기는 9%로 전체 기업 중 4번째로 높았다.2020년 기준 국내 바이오 중소벤처기업 현황 통계 일부발췌결국 이 같은 통계 지표를 봤을 때 바이오 중소벤처기업은 매출액 대비 연구개발비 투자가 가장 높았지만 구조상 매출액 대비 순이익을 기대하기 어려운 상황이라는 것으로 설명 가능하다.여기에 더해 IPO까지 걸리는 소요기간이 의약품 분야 기준 평균 9.4년이 걸린다는 점을 고려했을 때 투자 한파 속에서 투자금 확보에 대한 방안 고민이 더 깊어질 것으로 보인다.특히, 올해 전 세계적인 경제 한파로 제약바이오산업 투자와 관련해 보수적인 시각과 2022년 대비 투자 흐름이 나아질 것이라는 시각이 공존하고 있는 상황.이에 대해 투자 전문가들은 경색된 투자 흐름 속에서 M&A 등 노선 다변화의 목소리도 꾸준히 내고 있는 상황이다.BNH 인베스트먼트의 파트너 강지수 전무는 "회사가 생존하는 것이 중요하기 때문에 현금이 바닥나지 않는 것을 목표로 프로젝트의 우선순위를 결정한 뒤 집중하는 게 필요할 것 같다"며 "기술이전이나 M&A 등 무엇을 목표로 하던 기업 입장에서는 하고 싶은 연구만 해서는 안되고 투자자가 살 수 있는 매력적인 회사를 만드는 노력을 해야 한다는 의미"라고 밝혔다.바이오업계 관계자는 "코로나 기간 동안 바이오산업 투자 상황이 달라진 면이 있지만 중소벤처가 가지고 있는 고민을 보여주는 통계지표로 보인다"며 "중소바이오벤처가 바이오 생태계에서 가장 많은 비중을 차지하는 만큼 보릿고개를 넘고 자생력을 갖추기 위한 지원이 필요하다고 본다"고 덧붙였다.