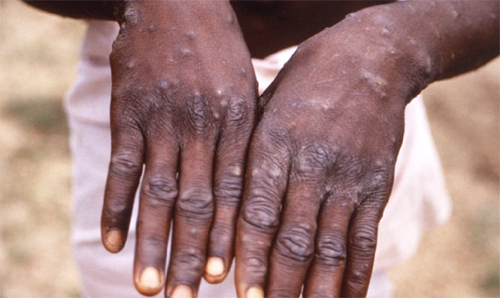
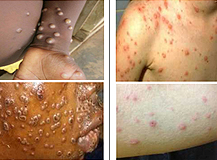
"더 쎈 놈이 온다" 경쟁 치열해지는 항체 건선약 시장
메디칼타임즈=원종혁 기자 이중억제기전을 가진 '표적 건선 신약(항체의약품)'이 현행 생물학적제제 대형품목인 '휴미라'와의 직접비교를 단행하며 우월성 검증에 마침표를 찍었다.
휴미라를 투약받다 약물치료를 전환한 환자에서도 피부병변 개선혜택을 최대 1년간 유지했다는 대목과, 중증 부작용 발생에 있어서도 합격점을 받아 추후 후발 경쟁에 귀추가 주목되는 이유다.
더욱이 인터루킨-17A와 F(IL-17A, F)를 선택적으로 억제하는 이중 특이적 단일클론항체약인 '비메키주맙(bimekizumab)'이 겨냥한 시장이, 현재 건선 치료제 시장을 리딩하고 있는 IL-17A 억제제 '코센틱스(제조사 노바티스)'와 '탈츠(제조사 릴리)' 등이 포진하고 있다는 점도 계열약 경쟁에 이목이 쏠린다.
계속되는 신약의 추가로 항체 건선약 시장이 점점 더 치열한 경쟁을 예고하고 있다.
비메키주맙의 직접비교(헤드투헤드) 3상임상인 'BE SURE 연구'의 최종 분석 결과, 대조군으로 잡혔던 휴미라(아달리무맙)에 우월성 검증을 끝마쳤다.
이미 작년말, 비메키주맙은 주요 분석결과 일부를 선보이면서 우월성 비교에 가능성을 던졌는데 전체 세부 데이터 공개는 이번이 처음이었다. 해당 구연발표 자료는 29일부터 31일(현지시간)까지 온라인으로 진행된 올해 유럽피부과학회(European Academy of Dermatology and Venereology Congress) 연례회의에서 논이됐다.
개발사인 UCB제약은 작년 10월 비메키주맙과 얀센의 판상 건선 치료제인 '스텔라라'의 효능을 직접 저울질한 3상임상 'BE VIVID 연구'에서도 우월성을 입증한 바 있다. 결과적으로 IL-12 및 IL-23을 선택적으로 억제하는 스텔라라에 이어, TNF 억제제인 휴미라와의 비교에서까지 앞선 혜택을 확보했다는 얘기다.
현재 국내에서도 인터루킨 억제제 계열 건선약 시장은, 선발품목인 얀센 스텔라라(우스테키누맙)에 뒤이어 노바티스 '코센틱스(세쿠키누맙)', 얀센 '트렘피어(구셀쿠맙)', 릴리 '탈츠(익세키주맙)', 애브비 '스카이리치(리산키주맙)' 등이 처방경쟁에 가세하면서 400억원 규모로 몸집을 불리고 있다.
실제 올해 상반기까지 누적 매출실적(IQVIA 기준)을 보면, 스텔라라 127억원, 코센틱스 86억원, 트렘피어 55억원, 탈츠 22억원 등으로 집계됐다.
피부병변 개선 지속효과 우월해 "중증 이상반응 휴미라 더 높아"
일단 이번 학회에 발표된 비메키주맙 BE SURE 최종 분석자료는, 두 가지 측면에서 건선 치료제로의 혜택을 분명히 했다.
피부 병변의 90% 이상이 개선된 건선 영역과 중증도 지수(PASI 90) 및 피부 투명도를 평가하는 국제평가지표(IGA)를 놓고, 치료 16주차에 아달리무맙과의 비교에서 모두 앞선 결과지를 보인 것이다. 더불어 치료 16주 및 24주차 PASI 100 지표 비교도 마찬가지였다.
특히, 연구시작 당시부터 비메키주맙으로 치료를 시작한 환자군의 경우 최대 1년까지 치료 반응률을 유지한 것으로 나타났다. 또 아달리무맙에서 비메키주맙으로 약물치료를 전환한 경우(스위칭 환자군)에서도 피부 병변해소 반응 속도가 증가한 것이다.
책임저자인 영국 맨체스터의대 리차드 와렌(Richard Warren) 교수는 발표를 통해 "건선 치료제로 가장 흔하게 사용되는 약제와의 비교에서 유의한 데이터를 확인했다는 것이 임상의 핵심"이라며 "약제 전환군에서도 이러한 치료혜택을 보고한 것도 시사하는 바가 크다"고 평가했다.
세부 데이터를 살펴보면, 비메키주맙 치료군에서는 치료 16주차 PASI 90 지표와 관련해 86.2%를, 휴미라 치료군에서는 47.2%를 나타냈다. IGA 0/1 지표를 놓고는 비메키주맙 치료군 85.3%, 휴미라 치료군에서는 57.2%를 보고했다.
무엇보다, PASI 100 지표 달성률에서는 두 배 이상의 격차를 확인했다는 대목이다. 치료 16주차 PASI 100 지표는 비메키주맙 치료군 60.8%, 휴미라군 23.9%였으며 치료 24주차까지 연장한 경우에서도 각각 66.8%와 29.6%로 상당한 차이가 관찰됐다.
더불어 복합 평가지표였던 PASI 90, PASI 100 및 IGA 0/1 지표 비교에서도, 비메키주맙 투약군에서는 치료 56주차까지 이러한 반응률을 유지했다. 아달리무맙에서 비메키주맙으로 치료를 전환한 환자군도 예외는 아니었다.
안전성과 관련해서는 치료로 인한 응급이상반응 발생률(TEAEs)은 비슷한 수준을 보고했다.
치료로 인한 응급이상반응 및 중증 TEAEs 발생률은 비메키주맙 치료군이 71.5%, 1.6%였으며, 휴미라 치료군에서는 69.8%, 3.1%로 중증 이상반응 발생은 오히려 휴미라 치료군에서 다소 높게 나타났다.
이와 관련해 가장 흔하게 관찰된 이상반응은 인후두염(20.9%)을 비롯한 구강 칸디다감염증(16.2%), 상기도 감염증(9.0%) 순이었다. 이외 자살 행동이나 염증성 장질환, 주요심장사건(MACE) 발생 등의 중증 부작용은 관찰되지 않았다.
한편 건선 치료제 시장에서 IL-17A 억제제들의 처방 적응증 경쟁도 치열한 상황이다. 코센틱스는 판상 건선 및 건선성 관절염, 강직성 척추염을 적응증으로 가지고 있는 가운데, 릴리의 탈츠는 작년 10월 강직성 척추염을 적응증으로 추가 확대받으며 코센틱스와의 경쟁구도를 분명히 했다.
이번 임상을 발표한 비메키주맙은, 현재 건선 이외에도 건선성 관절염 및 강직성 척추염, 비방사선학적 척추관절염에서 임상을 진행하고 있으며 오는 2021년 말경 임상자료가 차례로 공개될 예정이다.