초점
"케이캡 독주 잡아라" 잇따른 도전장에 P-CAB 시장 후끈
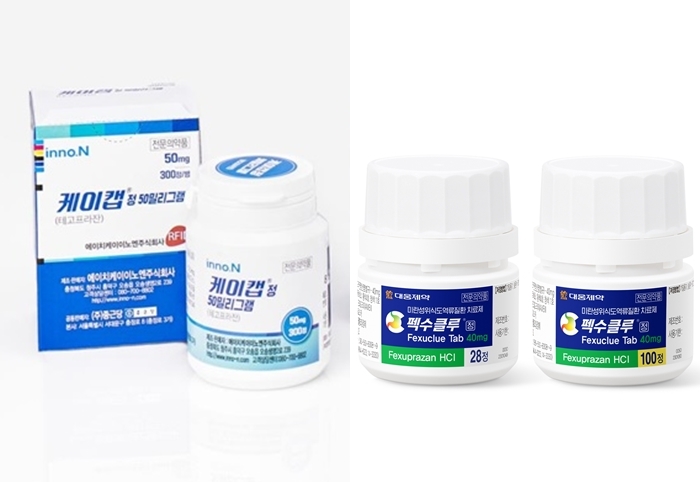
메디칼타임즈=허성규 기자케이캡으로 대표되는 'P-CAB' 시장에 후발주자들이 연이어 도전장을 내밀면서 시장이 과열 양상으로 치닫고 있다.HK이노엔과 대웅제약이 시장을 지배하고 있는 상황에 제일약품이 가세하며 3파전을 예고한데 이어 후발로 시장에 진출하기 위한 움직임이 이어지면서 치열한 경쟁을 예고하고 있는 것.6일 제약업계에 따르면 지난 2월 케이캡에 대한 특허 도전이 첫 승소을 거둔 이후 인용 심결을 받는 기업들이 점차 늘고 있는 것으로 확인됐다.■후발주자들 제네릭 공략…실제 출시까진 글쎄이러한 특허 도전은 시장에서 높은 성장세를 보이고 있는 HK이노엔의 케이캡을 잡기 위한 국내 제약사들의 움직임으로 풀이된다. 하루 빨리 제네릭을 내놓기 위해 케이캡의 특허를 집요하게 공략하고 있는 셈이다.위식도역류질환 시장에서 입지를 강화하는 P-CAB 제제 시장의 경쟁이 점차 복잡한 양상을 띄고 있다.이는 지난 2022년 12월 삼천당제약이 케이캡의 '벤즈이미다졸 유도체의 신규 결정형 및 이의 제조방법' 특허(2036년 3월 12일 만료, 이하 결정형특허)에 도전하면서 시작됐다.이후 국내사들이 속속 해당 특허에 도전하면서 각 제약사별로 적게는 1건, 많게는 4건의 심판을 청구한 상황. 전체적으로는 약 80여개사에 달하는 기업들이 도전에 나섰다.시간이 지나며 일부 취하를 선택한 기업들도 있지만 최종까지 70개사가 넘는 제약사들이 특허에 도전했고 지난 2월 삼천당제약을 비롯해 총 59개사가 청구 성립 심결을 받아내며 마침내 특허 일부가 무너졌다.이후에도 승소는 이어지고 있다. 지난 4월은 물론 5월 1일에도 추가적으로 청구 성립 심결을 받아내면서 제뉴원사이언스 등 일부 제약사를 제외한 대부분의 제약사들이 일차적으로 특허 회피에 성공했다.여기에 후발 주자들의 승소가 이어지고 있다는 점에서 남은 제약사들 역시 특허 회피에 성공할 것이라는 예상이 지배적인 상황.HK이노엔 역시 방어에 나선 상태다. 이같은 결과에 대하 연이어 항소를 진행하며 특허를 방어하고 있기 때문이다. 이와 관련한 소송이 지속적으로 이어질 수 밖에 없는 이유다.케이캡 외에도 국내사들의 P-CAB에 대한 도전은 확대되고 있는 모습이다.이는 국내 허가는 획득했으나 출시는 되지 않은 다케다제약의 보신티에 대한 국내사들의 관심 역시 늘고 있는 상황이기 때문이다.다케다제약의 보신티는 지난 2019년 3월 허가된 품목으로 케이캡에 이어 두 번째로 국내에서 허가된 P-CAB제제다.하지만 급여 등재에 실패하면서 국내 출시가 불발된 상황. 그러자 국내사들에 해당 품목의 제네릭 개발을 통해 활로를 찾고 있는 셈이다.실제로 지난해 이미 동화약품, 대원제약, 한림제약, 동구바이오제약, 마더스제약, 비씨월드제약 등이 보신티의 제네릭 출시를 위한 생동 시험을 승인 받은 바 있다.또한 올해에도 한국휴텍스제약, 동국제약, 비보존제약, 유니메드제약, 노바엠헬스케어 등도 생동을 승인 받으며 개발에 참여하는 회사들이 늘고 있다.문제는 특허 도전이나 생동 모두 현 시점에서는 빠른 결과를 얻어내기는 어렵다는 점이다.HK이노엔의 케이캡은 결정형 특허 외에도 2031년 8월 만료되는 '크로메인 치환된 벤즈이미다졸 및 이들의 산 펌프억제제로서의 용도' 특허(이하 물질 특허)가 남아있다.결국 후발 주자들이 승기를 잡기는 했지만 실제 특허를 완전히 회피해 제네릭을 출시하기 까지는 시간이 더 걸릴 수 밖에 없는 셈이다.또 보신티 역시 재심사 기간이 2025년 3월 28일까지 인데다가 2027년 12월 20일 만료 특허와 2028년 11월 17일 만료 특허 등을 여전히 보유한 상태에 있다.P-CAB 시장을 이끌고 있는 HK이노엔의 케이캡(좌)과 대웅제약의 펙수클루(우)■허가 이후에는 적응증·글로벌에 박차…선두주자 입지 강화이에 따라 현 시점에서는 시장을 지배하고 있는 HK이노엔의 케이캡과 대웅제약의 펙수클루, 또 곧 시장에 진입할 것으로 예상되는 온코닉테라퓨틱스의 자큐보가 경쟁을 이어갈 수 밖에 없다.이에 따라 이들 기업은 모두 적응증 등 확대를 통해 시장 입지를 다지고 새로운 경쟁력을 확보하기 위해 안간힘을 쓰고 있다.우선 가장 먼저 시장에 진입한 케이캡의 경우 시장 진입 이후 적응증 확대와 제형 변화 등을 이어왔다.케이캡은 현재 기존 50mg 정제에 더해 25mg 저용량 품목을 허가 받았으며, 이후 2개 용량의 구강붕해정까지 허가 받았다.적응증 역시 △미란성 위식도역류질환의 치료 △비미란성 위식도역류질환의 치료 △위궤양의 치료 △소화성 궤양 및/또는 만성 위축성 위염 환자에서의 헬리코박터파일로리 제균을 위한 항생제 병용요법 등과 저용량에 한정된 △미란성 위식도역류질환 치료 후 유지요법 총 5개까지 늘린 상태다.펙수클루 역시 허가 이후 저용량을 추가로 출시하며 기존 △미란성 위식도역류질환의 치료에 더해 저용량에 한한 △급성위염 및 만성위염의 위점막 병변 개선 등의 적응증을 확보했다.이들은 추가적인 적응증 확대에 박차를 가하고 있으며 대웅제약은 미란성 위식도역류질환 치료 후 유지요법과 비스테로이드성 소염진통제(NSAIDs)로 인한 궤양 예방은 물론 중국에서 헬리코박터균 제균 치료 임상을 신청했다.케이캡 역시 비스테로이드성 소염제(NSAIDs) 병용투여 요법 등의 적응증 확대를 꾀하고 있다.또한 최근 허가 받은 온코닉테라퓨틱스의 자큐보정 역시 허가 이후 빠르게 추가 임상을 진행하며 적응증 확대에 나서고 있다.온코닉테라퓨틱스는 지난 24일 허가 이후 NSAIDs 유도성 소화성궤양 예방 임상 승인받으며 적응증 확대를 꾀하고 있는 상태다.아울러 선두주자인 케이캡과 펙수클루 모두 글로벌 시장 진출을 위한 노력을 지속하고 있는 상태다. 케이캡은 최근 중동과 북아프리카 지역으로 확대를 포함해 총 45개국에 기술수출 또는 완제품 수출 형태로 진출에 성공했고 펙수클루는 역시 출시 후 1년 6개월여만에 전 세계 24개국에 지출했다.영업전도 눈여겨 볼 관전 포인트다. 국내에서 케이캡과 펙수클루 모두 올해부터 각기 다른 제약사와 파트너십을 체결하며 영업전에 나섰기 때문이다.우선 케이캡은 기존에 협력하던 종근당과의 계약이 종료 된 이후 보령과 손잡고 카나브-케이캡 공동 판매 전선을 구축했다. 또한 대웅제약은 종근당과 다시 협력 펙수클루의 공동 판매에 나섰다.따라서 앞으로도 P-CAB 제제 시장은 경쟁 과열 상태가 이어질 가능성이 높다. 앞서 제네릭 개발이 이어지는 다케다제약의 보신티는 물론 일동제약이 개발 중인 신약 역시 출시가 가시화되고 있는 이유다.실제로 P-CAB 제제가 국내에서 폭발적으로 성장하면서 원 개발사인 다케다제약이 국내 도입 가능성을 놓고 검토를 진행 중인 것으로 파악됐다.일동제약 역시 지난 2월 미란성 위식도 역류질환 환자에 대한 'ID120040002'의 임상 2상을 승인 받으며 허가에 속도를 내고 있다.이에 따라 과연 현재 3파전이 굳어진 P-CAB 제제 시장에 얼마나 많은 제약사들이 지속적으로 도전을 이어갈지, 또한 이들의 참전이 과연 시장에 어떠한 영향을 미칠지에 제약계의 관심이 모아지고 있다.