기획
처방권 진입 5주년 맞은 면역항암제...안전성 이슈 결론은?
메디칼타임즈=원종혁 기자 '키트루다(펨블롤리주맙)' '옵디보(니볼루맙)' '티쎈트릭(아테졸리주맙)' 등 면역관문억제제로 불리는 면역항암제들이 처방권 진입 5주년을 맞은 가운데 안전성 결과가 속속 모습을 드러내고 있다.
처방 경험이 쌓이면서 효과에 가려진 안전성 이슈가 하나 둘 확인되고 있는 것인데, 환자나 의사 모두 각별한 관심이 필요한 상황이다.
때마침 최근 열린 미국임상종양학회 면역항암심포지엄(ASCO-SITC) 자리에서도 면역항암제를 투여받은 암환자에서 갑상선 기능장애와 정맥혈전색전증 발생을 조사한 5년차 리얼월드 임상 데이터가 구두발표되며 학계 이목을 집중시켰다.
앞서 2015년 면역항암제들이 시장에 처음 등장했을 당시에도, 약물 내성이나 독성 문제는 꾸준히 제기되어 왔다.
실제 처방 초기 보고된 증례들을 살펴보면, 면역항암제를 사용한 환자에서는 주로 드문 부작용들이 보고됐다. 이를테면 1000명중 1명 꼴로 발생이 예상되는 당뇨병성 케톤산증으로 중환자실 치료를 필요로 하는 환자들이 있었고, 자가면역뇌염를 비롯한 소수 환자에서 폐렴 등이 관찰됐기 때문이다.
이를 두고 많은 전문가들은 면역항암제 허가의 토대가 된 제약사 주도 임상 데이터들의 경우, B형간염을 비롯한 결핵 경험, 뇌전이, 자가면역질환, 심각한 통증 등을 동반한 환자 등 실제 진료현장에서 마주하는 환자군들이 임상 연구에 거의 포함되지 않았다는 점을 지적했었다.
따라서 면역항암제를 사용하는데 있어 혹시 모를 안전성 이슈들을 예방하고자, 처방 병원들의 다학제적 시스템 마련과 독성관리 가이드라인 제정이라는 안전망 구축을 주장한 바 있다.
진입 5년째를 맞은 현재, 광범위하게 처방 중인 면역항암제를 사용한 환자들에서 나타나는 이상반응은 '갑상선 기능장애' 문제와 '정맥혈전색전증(VTE)' 발생 위험이 기정 사실화되고 있다. 최근 발표된 리얼월드 연구에 따르면, 갑상선 기능장애의 경우 전체 374명 환자에서 면역항암제 치료를 진행한 159명 환자에서는 갑상선 기능장애가 보고됐다.
이러한 현상은 실제 다양한 임상들에서도 공개된 바 있다. 키트루다의 대표적인 'KEYNOTE 연구'나 옵디보의 'CHECKMATE 연구'들에서도 갑상선 기능장애가 발생한 환자들의 비율은 6%~18% 수준이었던 것.
서울대병원 종양내과 김범석 교수는 "면역항암제를 둘러싼 사회 문화적인 현상은, 조심스러운 측면이 많다. 면역학적 독성반응은 기존 세포독성항암제나 표적치료제들과는 양상이 판이하게 다르다"고 설명했다. 그러면서 "제약회사 주도 임상시험은 굉장히 제한적으로 이뤄지기 때문에, 무엇보다 실제 처방환경에서의 리얼월드 데이터 수집이 관건"이라며 부작용 보고의 중요성을 강조했다.
이슈1. 면역항암제 3종 "치료 3개월 이후 갑상선 기능이상 보고"
ASCO-SITC에서는 후향적 분석을 통해 이러한 내용이 재확인됐다.
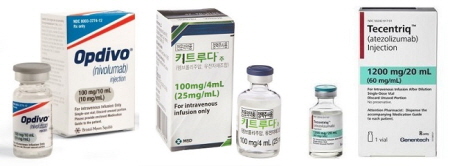
임상에 등록된 환자들은 2015년 4월부터 2019년 8월까지 면역항암치료를 진행한 환자였고, 치료 시작 전에 갑상선 기능검사를 시행했다. 여기엔 키트루다(펨브롤리주맙) 투약군 55명, 옵디보(니볼루맙) 투약군 81명, 티쎈트릭(아테졸리주맙) 투약군 23명 등 총 159명의 환자들이 갑상선 기능장애를 보고한 것으로 나타났다.
사진: 면역항암제 옵디보(좌), 키트루다, 티쎈트릭(우).
특징적으로 이들 대부분은 자가 치유가 가능한 '1등급(grade 1)'에 해당하는 이상반응을 보고했으며, 환자 누구도 갑상선 기능장애로 인해 갑상선기능저하증에 주로 사용되는 합성 갑상선호르몬 약물인 '레보티록신(levothyroxine)' 치료를 시행하지 않았다.
또 한가지 주목할 점은, 이러한 비정상적인 갑상선 기능장애는 면역항암제 치료를 시작한지 3개월 이후에 보고가 됐다는 대목이다.
먼저 아테졸리주맙의 경우 갑상선 기능장애와 관련해 1등급 이상반응에 해당하는 갑상선염이 73.9%에서 보고됐으며, 2등급(grade 2) 갑상선 이상반응은 21.2%에서 나타났다. 더불어 평균적으로 갑상선염은 치료 97.3일차에 발생했다.
니볼루맙도 크게 다르지는 않았다. 니볼루맙 치료군에서는 1등급 이상반응은 56.4%, 2등급 이상반응은 32.1%로 관찰됐다. 니볼루맙 투약군에 갑상선 기능장애는 평균 84.2일차에 보고가 이뤄졌다.
펨브롤리주맙 치료군에서는 1등급 갑상선 이상반응이 76.4%, 2등급 이상반응은 21.8%로 나타났다. 마찬가지로 펨브롤리주맙 치료 120.45일차에 이러한 갑상선 기능장애가 발생한 것으로 분석했다.
책임저자인 미국이스트캐롤라이나의대 헤더 브로디(Heather Brody) 교수(비덴트메디칼센터)는 "단일기관 후향적 분석 결과에서는 갑상선 기능장애를 보고한 비율이 42.5%로 나타났다. 이는 이전에 보고된 것보다 높은 수치"라면서 "하지만 대부분의 이상반응이 스스로 해결이되는 1등급 이상반응 수준이었다. 이들 중 10명만이 해당 갑상선 질환으로 인한 치료를 필요로 하는 환자였다"고 설명했다.
그럼에도 "면역항암제 치료를 중단하거나 지속하는데 있어 이러한 갑상선 기능이상은 정상으로 돌아올 수 있다는 사실은 발견했다"며 "후향적 분석결과에서도 갑상선 기능이상으로 면역항암제 치료를 중단해야 하는지가 나타나지 않았는데, 면역항암제를 투여받은 환자들에서 보고되는 이러한 갑상선 기능변화가 일시적인 문제인지, 치료가 필요한 안전성 문제이지에 대해선 추가적으로 평가를 진행해나갈 계획"이라고 덧붙였다.
이슈2. 흑색종에 옵디보+여보이 병용 "치료 12개월 이내, VTE 발생 가장 높아"
이어 9일(현지시간) 구두 발표된, 흑색종 환자에서 면역항암제 병용요법을 진행할 경우 정맥혈전색전증(venous thromboembolism, 이하 VTE) 발생 위험이 증가했다는 안전성 평가 결과도 주목해볼 데이터다(초록번호 94).
특히, 옵디보(니볼루맙)와 여보이(이필리무맙) 병용요법을 진행한 환자들에서는 VTE 발생 위험이 가장 높았다는 평가다.
책임저자인 클리브랜드 타우씨그암센터 타마라 서스만(Tamara A. Sussman) 박사는 "암환자들에서 VTE의 발생은 사망률과 전반적인 예후를 안좋게 만드는 인자로 꼽힌다"면서 "면역항암제 치료를 받는 흑색종 환자에서 이러한 VTE 유병률은 아직까지 구체적인 데이터가 나오지 않은 상황"이라고 소개했다.
연구를 살펴보면, 클리브랜드 암센터에서 2015년 7월부터 같은해 12월까지 면역관문억제제를 처방받는 흑색종 환자 219명의 의무기록을 분석대상으로 잡았다. 이들 중 79.9%가 원격 전이가 이뤄진 흑색종 환자들이었으며, 16.4%는 뇌전이가 진행된 환자들이었다.
그 결과, 니볼루맙과 이필리무맙을 병용한 환자군 59명 가운데 12명(20%)이 VTE 유병을 나타냈다. 이어 이필리무맙을 단독으로 사용한 환자군 48명 가운데 6명(13%)이 VTE가 발생했고, 니볼루맙 단독요법은 32명 환자 중 4명으로 13%의 발생률을 보였다.
더불어 키트루다(펨브롤리주맙) 단독 치료군 80명에서도 9명(11%)의 환자들이 VTE 발생을 경험한 것으로 나타났다.
주목할 점은, 이러한 VTE 발생이 면역항암제 치료를 시작한 후 대개 첫 12개월 이내에 보고됐다는 대목이다. 더불어 원격전이가 진행된 환자들에서 VTE 발생 시점이 앞당겨졌는데, 특히 니볼루맙과 이필리무맙을 병용한 환자군에서는 VTE 발생 시점이 4.9개월(중간값)로 다른 면역항암제를 사용한 경우 9.3개월에 비해 유의한 차이를 보인 것이다.
이 밖에도 뇌전이가 없는 환자들에서는 VTE 발생과 전체 생존율(OS) 악화 사이에는 유의한 연관성이 포착됐다.
연구팀은 발표를 통해 "6개월간 VTE 발생없이 생존율을 비교한 결과 니볼루맙과 이필리무맙 병용군에선 18.5%로, 면역항암제 단독치료를 시행한 환자군 71.8% 대비 낮게 나온 것도 주목해야 한다"면서 "추후 연구에서는 해당 환자들에서 혈전 색전증 예방치료를 시행하는것이 어떠한 혜택이 있는지도 평가해볼 필요가 있을 것"으로 전했다.