삼첨판 치환술 시장 경쟁 돌입…에드워즈와 애보트 맞불
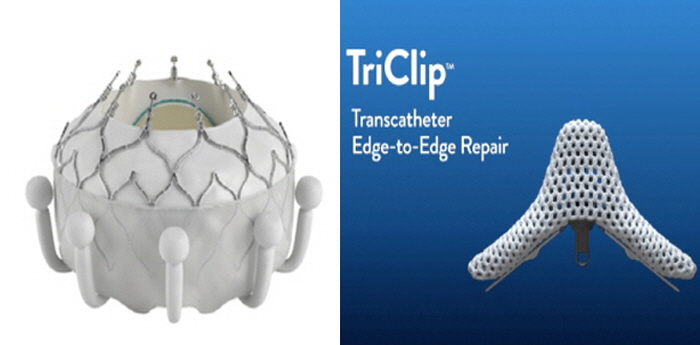
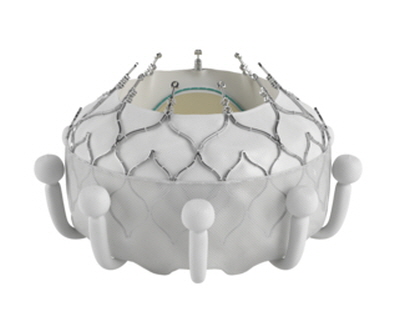
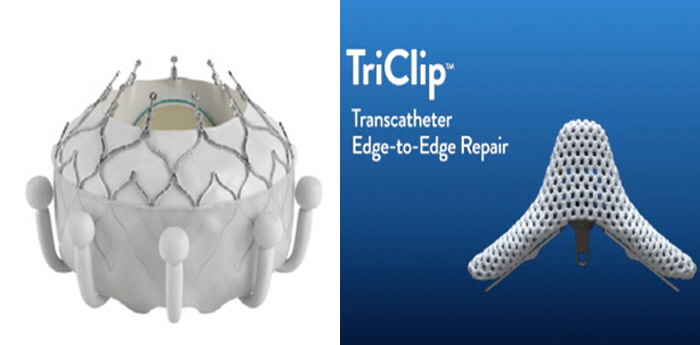
메디칼타임즈=이인복 기자기술적 한계로 오랜 기간 미개척 상태로 남아있던 경피적 삼첨판막 치환술(TTVR) 분야에 글로벌 의료기기 기업들이 잇따라 깃발을 꽂으며 시장을 열어가는 모습이다.에드워즈라이프사이언시스가 세계 최초로 미국 식품의약국(FDA) 승인을 받고 시장을 선점한지 두달만에 애보트가 곧바로 승인을 통해 추격에 나서면서 본격적인 경쟁 구도가 형성되고 있는 셈이다.에드워즈라이프사이언시스와 애보트가 삼첨판 치환술을 놓고 경쟁에 돌입했다(사진 왼쪽부터 이보크와 트라이클립).현지시각으로 4일 FDA는 애보트의 경피적 삼첨판막 치환술 장비인 트라이클립(TriClip)을 최종 승인했다.트라이클립은 삼첨판 역류(TR) 또는 누출을 치료하기 위한 장비로 카테터 방식을 통해 다리 정맥을 통해 치료를 진행한다.삼첨판막은 대동맥 판막 질환과 달리 아직까지는 개흉 수술 외에 다른 치료법이 존재하지 않았던 것이 사실.인체 구조적 한계가 명확했던데다 승모 판막이나 대동맥 판막 질환에 비해 환자군이 적다는 점에서 미개척 분야로 남아있던 셈이다.또한 대동맥 문제를 해결하면 삼첨판 문제도 자연스레 해결할 수 있다는 것이 정설로 오랜 기간 유지되면서 이에 대한 수요도 적었다.그러나 이러한 학설이 뒤짚히고 삼첨판 문제로 고통받는 환자들이 늘면서 이 분야에 대한 개척이 시작됐다.먼저 시장을 연 것은 경피적 대동맥 판막 치환술(TAVI)를 개척하며 표준 치료법으로 올려 놓은 에드워즈라이프사이언시스다.올해 2월 경피적 삼첨판 치환술 시스템인 이보크(EVOQUE)가 세계 최초로 FDA 문턱을 넘어서며 시장을 열었기 때문이다.이보크는 전향적 글로벌 다기관 연구인 'TRISCEND'를 통해 유효성과 안전성을 입증받았다. 이 임상에서 이보크로 시술받은 환자는 30일, 6개월, 1년에 걸친 추적 관찰 결과 90.1%의 생존율과 88.4%의 심부전 위험 감소 효과를 인정받았다.또한 중증도 이상의 기능적, 퇴행성 삼첨판 역류(TR)을 가지고 있던 환자의 97.6%가 유의미한 역류 감소 효과가 나타나며 학계의 주목을 받았다.하지만 이같은 독점은 오래가지 못했다. 지난 3월 FDA 자문위원회가 애보트의 트라이클립에 대한 승인 신청 회의를 열고 만장일치로 안전성과 유효성을 인정했기 때문이다.당시 자문위원 14명 중 12명이 트라이클립의 유효성을 인정했으며 안전성 부분에 대해서도 13대 1로 압도적 찬성표를 던졌다.이를 기반으로 FDA가 마침내 4월 트라이클립에 대한 최종 승인을 내면서 세계 두번째 삼첨판 치환술 시스템이 세상에 나온 셈이다.트라이클립은 'TEER'와 'TRILUMINATE' 임상을 통해 안전성과 유효성을 인정받았다. 이 임상에 따르면 등록 환자의 87%에서 삼첨판막 역류(TR)가 개선되는 결과가 나왔다.이에 따라 불과 작년까지 미개척 분야로 남아있던 삼첨판 치환술 분야에서 글로벌 기업들이 본격적인 경쟁을 펼칠 것으로 보인다.특히 에드워즈라이프사이언시스와 애보트 등 두 회사 모두 TAVI를 비롯해 심혈관 분야에서 경쟁을 펼치고 있다는 점에서 전장이 보다 넓어질 것으로 전망된다.따라서 과연 에드워즈라이프사이언시스가 TAVI에 이어 삼첨판 분야에서도 분야 최강자로 자리를 굳힐지 보다 많은 네트워크를 가진 애보트가 반전을 이룰 수 있을지에 관심이 모아지고 있다.