MARIPOSA 하위 분석서 전체 연구와 일관된 생존율 혜택 입증
J&J-유한양행 영업‧마케팅 내년 본격화, 급여 협업체계 구축 주목

EGFR 변이 비소세포폐암 1차 치료에서 리브리반트-렉라자 병용요법이 전체 환자군에 이어 아시아 환자에서도 생존 혜택을 그대로 재현했다. 글로벌 임상3상 MARIPOSA 연구의 아시아 하위분석 결과, 병용요법은 오시머티닙 단독요법 대비 전체생존기간(OS)을 개선하며 '표준치로' 근거를 차곡차곡 쌓아나가고 있다.
국내 상황을 본다면 내년부터 본격적으로 리브리반트(아미반타맙) 병용요법의 판권을 보유한 존슨앤드존슨(한국얀센)과 렉라자(레이저티닙) 개발사인 유한양행이 손을 잡고 임상현장 영업‧마케팅이 나설 전망이다.
아시아 생존 혜택 입증, 경쟁옵션과 차별화
일본 긴키의대(Kindai University Faculty of Medicine) 히데토시 하야시(Hidetoshi Hayashi) 교수는 지난 6일(현지시간) 싱가포르에서 열린 유럽임상종양학회 아시아(ESMO ASIA 2025) 연례학술대회에서 MARIPOSA 3상 연구 하위 분석 결과를 발표했다.
앞서 J&J는 올해 3월 열린 유럽폐암학회에서 리브리반트-렉라자 병용요법 OS 업데이트 결과를 핵심으로 한 임상3상 결과를 공개한 바 있다.
당시 발표에 따르면, 리브리반트-렉라자 병용요법군은 오시머티닙(아스트라제네카) 단독요법군 대비 사망 위험을 25% 낮췄다(HR, 0.75, 95% CI: 0.61–0.92, P<0.005). 병용요법군의 전체 생존기간 중앙값(mOS)은 도달하지 않았으며, NE(95% CI: 42.9–NE)로 분석됐고, 타그리소군은 36.7개월(95% CI: 33.4–41.0)로 확인됐다.
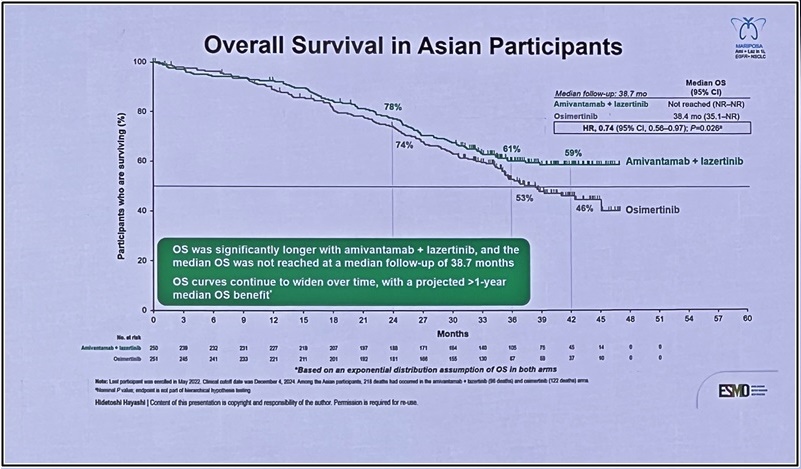
관심은 글로벌 임상 결과를 그대로 아시아 환자에서도 재현할 지 여부였다. 리브리반트-렉라자 병용요법의 적응증인 EGFR 돌연변이 비소세포폐암 환자가 아시아에서만 40~50%를 차지할 정도로 가장 많은 만큼 일관된 효과 달성이 중요할 수밖에 없는 대목이다. MARIPOSA 연구에 참여한 858명의 환자 중 501명이 아시아 환자이기도 했다.
공개된 하위 분석 결과에 따르면, 중앙 추적 관찰 기간 38.7개월 시점을 기준으로 렉라자-리브리반트 병용요법은 아시아인 환자의 전체 생존율(OS)에서 오시머티닙 단독요법에 비해 임상적으로 의미 있는 개선을 보였다. 렉라자-리브리반트 병용요법군 mOS는의 경우 아직 도달하지 않았고(NE; 95% CI, NE–NE), 타그리소 단독요법의 경우 38.4개월(95% CI, 35.1–NE)로 나타났다(HR, 0.74; 95% CI, 0.56–0.97, P<0.026).
결과적으로 연구진은 렉라자-리브리반트 병용요법이 오시머티닙 단독요법과 비교해 12개월 이상의 OS 개선효과가 기대된다고 평가했다.
이로써 경쟁 옵션으로 평가되는 오시머티닙-항암화학 병용요법의 중국 외 아시아인 하위분석 연구 결과와 단순 비교가 가능해졌다. 단순하게 평가했을 때 'HR 0.74'로 오시머티닙 단독요법보다 리브리반트-렉라자 병용요법이 큰 이득을 가져다준 점에서 임상현장 의료진이 주목할 수밖에 없는 부분이다.
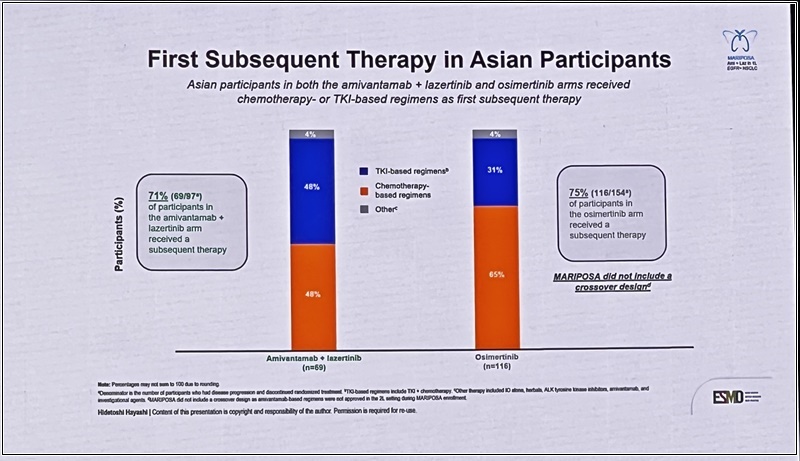
또 주목되는 점은 이번 하위 분석결과에서 나온 후속 치료(subsequent treatment) 패턴이다.
이번 하위 분석 결과를 보면, 리브리반트-렉라자 병용요법과 오시머티닙 단독요법 두 그룹 모두에서 첫 번째 후속 치료로 화학요법 또는 TKI 기반 요법을 70% 이상 받은 것으로 나타났다. 후속 치료 속에서도 일관된 OS 데이터가 도출 된 점을 주목하는 것으로 풀이된다.
익명을 요구한 한 제약업계 관계자는 "일부 연구 결과에서 서양인과 아시아인 다른 결과가 나온 것을 두고서 한국과 일본 등에서 이뤄지는 적극적인 후속치료를 배경으로 지목하기도 한다"며 "하지만 MARIPOSA 아시아 하위분석에서는 이 같은 후속 치료에도 불구하고 전체 임상결과와 일관된 데이터가 도출됐다는 점에서 의미를 둘만 하다"고 평가했다.
본격적인 협업체계 빛 볼까
이제는 이 같은 아시아인 하위 분석 데이터를 어떻게 활용할 것인지로 관심이 옮겨진다.
존슨앤드존슨과 유한양행이 뒤늦게나마 리브리반트-렉라자 병용요법을 공동판매하기로 합의한 만큼 향후 임상현장 영업‧마케팅에 적극 활용할 것으로 전망된다.
앞서 지난 10월 말 존슨앤드존슨 제약부문 국내 법인인 한국얀센은 유한양행과 '리브리반트–렉라자 병용요법'의 국내 판촉 활동을 공동으로 진행하기로 결정한 바 있다. 국내 식약처 허가 10개월 만에 이뤄진 양사의 합의다.

공동판매 합의 이전까지 리브리반트-렉라자 병용요법의 판촉 활동은 글로벌 판권을 보유하고 있는 존슨앤드존슨이 주도해 왔다. 존슨앤드존슨이 글로벌 판권을 보유한 만큼 당연한 조치였지만, 국산 신약이 포함된 병용요법인 만큼 유한양행을 행보도 주목을 받을 수밖에 없는 형국이었다.
자연스럽게 유한양행 또한 리브리반트-렉라자 병용요법의 자체 임상현장 영업‧마케팅을 자제해왔다. 자체적으로 진행하는 의료진 대상 제품설명회에서 조차 병용요법에서는 일절 언급을 하지 않았다는 후문이다.
내년도부터 본격적으로 이뤄질 양사의 공동판매가 어떤 시너지를 발휘할 수 있을지 주목되는 지점이기도 하다.
경쟁옵션은 정부의 항암제 병용요법 제도 개선의 효과로 상대적으로 고가인 치료제가 급여로 적용받고 있는 점도 리브리반트-렉라자 병용요법의 한계점으로 내년 풀어야 할 과제로 꼽힌다.
지난 9월 건강보험심사평가원 암질환심의위원회로부터 급여기준 미설정 판단을 받은 리브리반트의 급여 재도전 여부가 내년 핵심사항으로 여겨지는 이유이기도 하다.
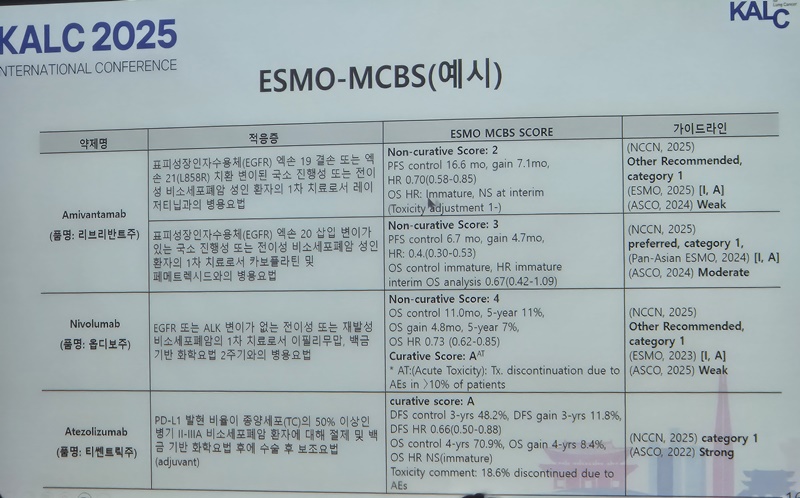
ESMO ASIA 2025에서는 리브리반트-렉라자 병용요법 아시아 하위분석과 함께 부작용 관리방안을 제시한 Cocoon 연구 아시아인 하위 분석 결과도 적극 활용할 것으로 예상된다.
해당 결과에 따르면, 예방적 피부관리(COCOON DM)군에서 2등급 이상 피부독성 발생률이 42%로, 77%를 기록한 표준관리(SoC)군 대비 절반 수준으로 낮아진 것으로 나타났다. 최근 심평원이 급여 적용 논의 과정에서 부작용 관리방안도 함께 살펴보고 있다는 점에서 주목할만한 부분이다.
심평원 김국희 약제관리실장은 "최근 암질심에 상정된 치료제의 급여기준 설정 논의 시 이상반응도 중요한 판단 요소가 됐다. 병용요법을 위주로 한 치료옵션이 늘어남과 동시에 이에 대한 논의가 자주 이뤄짐에 따른 것"이라며 "리브리반트-렉라자 병용요법도 마찬가지였다. 9월 논의 당시 치료효과와 함께 뒤따르는 이상반응 관리 문제가 대두되면서 해당 사항에서 감점의 근거가 됐었다"고 언급했다.