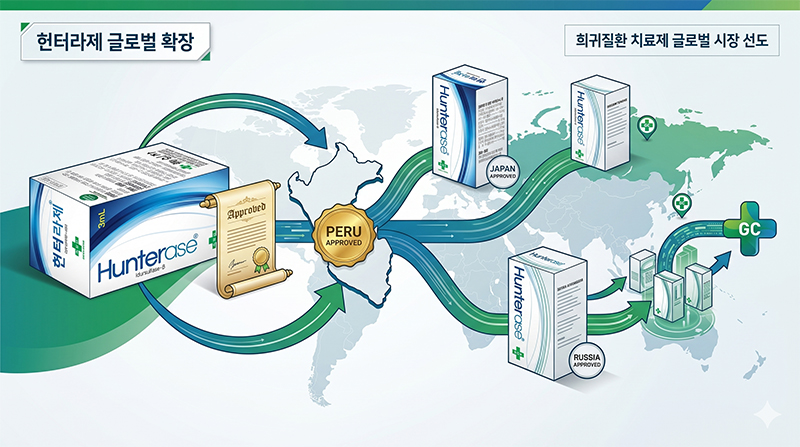
일본·러시아 이어 세번째 해외 승인…중남미 첫 교두보 마련
중증 환자 '미충족 수요' 해결하는 희귀질환 치료제 자리매김
[메디칼타임즈=이지현 기자] GC녹십자(대표 허은철)가 뇌실투여형(ICV, Intracerebroventricular) 헌터증후군 치료제 '헌터라제 ICV'의 페루 의약품관리국(DIGEMID) 품목허가를 획득했다고 6일 밝혔다.
이번 허가는 일본과 러시아에 이은 세 번째 글로벌 승인으로, GC녹십자의 희귀질환 치료제 포트폴리오가 중남미 시장으로 본격 확장되는 중요한 이정표가 될 전망이다.
헌터증후군은 IDS(Iduronate-2-sulfatase) 효소 결핍으로 인해 체내에 복합 당류인 글리코사미노글리칸(GAG)이 축적되는 선천성 희귀질환이다.
특히 전체 환자의 약 3분의 2는 중추신경계 손상을 동반하는 중증 형태로 나타나는데, 기존의 정맥주사(IV) 방식은 약물이 뇌혈관장벽(BBB)을 통과하지 못해 인지기능 저하 등 뇌 증상 개선에 한계가 있었다.
헌터라제는 약물을 뇌실 내로 직접 투여하여 뇌 조직 내 핵심 원인 물질인 헤파란 황산(HS)을 유의미하게 감소시킨다는 점이 차별화 포인트다.
이는 일본 임상 결과, 환자의 인지 및 발달 기능이 안정적으로 유지되거나 개선되는 경향이 확인됐으며 장기 추적 관찰을 통해 지속성까지 입증했다. 이와 더불어 월 1회 투약으로 편의성 측면에서도 높은 평가를 받고 있다.
헌터라제의 글로벌 진출에 주목하는 이유는 희귀질환 치료제로 고성장·고부가가치 분야라는 점이다. 실제로 희귀질환 치료제는 일반 의약품보다 약가가 높고 환자 충성도가 강해 안정적인 수익 창출이 가능하다는 점에서 매력적인 시장이다.
GC녹십자는 헌터라제를 통해 기존 표준 치료제의 한계를 넘어선 기술을 확보함으로써 희귀·중증환자 시장을 공략할 수 있는 구조다.
페루는 중남미 내에서도 규제 수준이 높은 국가라는 점에서 이번 승인은 브라질 등 인근 중남미 국가로의 추가 진출을 가속화하는 핵심 '레퍼런스' 역할을 할 전망이다. 다시 말해 이후 매출 증대로 이어질 가능성이 높다는 의미다.
GC녹십자는 기존 정맥주사형 '헌터라제 IV'와 시너지를 통해 환자 상태에 맞는 맞춤형 옵션을 제공함으로써 브랜드 지배력을 강화해나갈 것으로 보인다.
GC녹십자 이재우 개발본부장은 "확보된 장기 임상 데이터를 바탕으로 중증 헌터증후군 환자들의 미충족 의료 수요를 해소해 나갈 것"이라며 지속적인 글로벌 허가 확대 계획을 밝혔다.