'비교 유효성 임상 수행 결정 가이드라인' 제정
품질 중심 평가로 전환…개발 기간·비용 단축
[메디칼타임즈=허성규 기자] 식약처가 바이오시밀러의 임상 3상 요건 완화와 관련한 가이드라인을 내놓으며, 개발 기간 단축의 기대감을 높이고 있다.
이를 통해 개발 기간 단축과 비용 절감이 가능해지면서 바이오시밀러에 도전하는 제약사들이 늘어날 수 있을지 주목된다.
27일 식약처는 '동등생물의약품의 비교 유효성 임상시험 수행 결정 시 고려 사항' 민원인 안내서를 제정, 이를 공개했다.
이번 가이드라인은 바이오시밀러(동등생물의약품) 3상 임상시험인 비교 유효성 임상시험(CES)의 수행 여부를 결정할 때 고려해야 할 요소를 담고 있다.
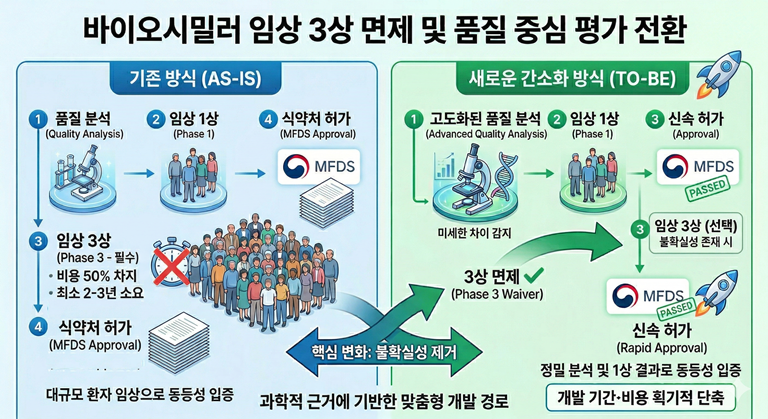
가이드라인의 주요내용은 ▲3상 요건 완화의 이론적 배경 ▲3상 임상시험 수행을 고려해야 하는 품질적 및 임상적 요소 ▲3상 임상시험 완화를 논의하는 절차 및 구비 자료 안내 등이며, 요건 완화를 적용하기 위한 관련 허가 규정도 개정할 예정이다.
또한, 업체가 바이오시밀러 개발 시 품질 자료와 1상 임상시험 결과를 기반으로 기허가된 오리지널 의약품과의 충분한 동등성과 안전성이 확보된 경우 3상 임상시험을 반드시 수행하지 않아도 되는 기준 등을 담았다.
즉 그동안 시행해온 바이오시밀러 임상 3상의 유용성을 재평가하고, 과학적 근거에 기반한 '맞춤형 개발 경로'를 제시하는 것이다.
이번 가이드라인의 핵심은 그간 축적된 바이오시밀러 허가 경험을 바탕으로, 고도로 발달한 물리화학적·생물학적 분석 기술이 환자를 대상으로 하는 임상시험보다 오리지널 의약품과의 미세한 차이를 더 민감하게 잡아낼 수 있다는 점을 공식화했다는 것이다.
제시된 임상 3상 면제 여부를 판단하기 위한 '유용성 평가 기준'을 살펴보면 전신 노출에 대한 약동학(PK) 평가가 가능해야 하며, 치료 용량이 용량-반응 곡선의 완만한 구간에 있어 미세한 품질 차이가 치명적인 결과로 이어질 가능성이 낮은 제품이어야 한다.
또한, 대조약의 데이터를 통해 면역원성이 안전성이나 유효성에 큰 영향을 미치지 않는다는 점이 확인되어야 한다.
다만, 안구 내 주사제처럼 전신 노출 확인이 어려워 PK 평가가 불가능한 제품이나, 작용기전이 복잡해 품질 분석만으로 불확실성을 해소하기 어려운 경우에는 기존처럼 비교 유효성 임상을 수행해야 한다.
여기에 사전검토 체계를 마련했다는 점에서 바이오시밀러의 신속한 개발 지원이 가능해진 만큼 국내사들의 진입 장벽 역시 한층 낮춰진 것으로 풀이된다.
이에 해당 요건 완화에 적용을 받는 바이오시밀러를 개발하고자하는 기업들은 기간 단축 및 비용 절감을 기대할 수 있게 될 것으로 보인다.
실제 바이오시밀러의 개발 과정에서 임상 3상의 진행은 비용의 50% 가량을 차지하는 장벽이었다는 점에서 업계의 기대감이 커질 수 밖에 없다.
특히 비교 유효성 임상시험은 수행에만 최소한 2~3년이 소요되는 만큼 비용적인 측면 뿐만 아니라 개발 기간 역시 단축 될 수 있을 것으로 예상된다.
여기에 최근 국내 뿐만 아니라 FDA에서도 바이오시밀러의 개발 과정에서의 요건 완화 등을 지속하고 있는 만큼 국내에서의 규제 완화는 글로벌 진출에도 도움이 될 것으로 전망이다.
반면 이같은 조치에도 실제 기술력을 보유한 기업의 영향력이 커질 가능성도 남아있다.
임상 3상을 건너뛰기 위해서는 1상 단계에서 모든 불확실성을 완벽하게 제거해야 한다.
결국 고도의 분석 역량과 정밀한 제조 공정 기술을 이미 확보한 선두 기업들이 훨씬 유리한 고지를 점할 가능성이 크다.
그런만큼 이번 임상 3상 요건 완화 속에서 실제 어떤 기업들이 추가적인 도전에 나설지, 또 이미 선두주자로 나선 기업들이 어떤 수혜를 보게 될지도 주목된다.