5년 간 치료 중단율 1% 미만…내성발생 0건
240주차까지 98%이상 바이러스 억제 효과 확인
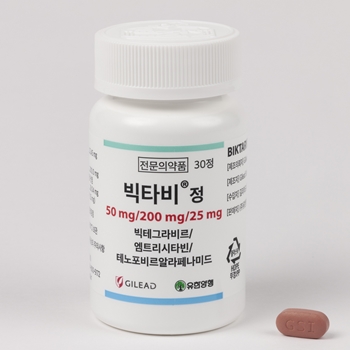
HIV-1 치료제 빅타비(성분명 빅테그라비르/엠트리시타빈/테노포비르알라페나미드, B/F/TAF)의 5년 장기 데이터가 허가사항에 추가됐다.
길리어드 사이언스 코리아는 지난 1월 30일 식품의약품안전처로부터 초치료 HIV-1 감염 성인을 대상으로 진행한 5년 장기 데이터 임상 정보가 추가됐다고 27일 밝혔다.
허가사항에 반영된 임상시험 정보는 이전에 항레트로바이러스 치료(Anti-Retroviral Therapy; ART) 경험이 없는 HIV-1 감염성인 634명 대상으로 빅타비의 유효성 및 안전성을 평가한 무작위배정, 이중맹검, 활성 대조군 3상 임상 2건(Study 1489 및 Study 1490 )의 5년 장기 추적 결과이다.
두 임상시험 모두 첫 투약부터 144주까지 이중맹검으로 평가한 후 선택적 연장 단계인 96주 동안 빅타비를 공개 라벨로 추가 투여했다.
Missing=Excluded (M=E)로 분석했을 때 두 임상시험의 1차 유효성 평가 변수인 48주 차 바이러스 수치 억제 효과(HIV-1 RNA 50 copies/mL 미만)는 빅타비 단독요법군에서 99% 이상으로 높게 나타났다.
이후 2차 유효성 평가 변수인 240주 차 바이러스 억제 효과에도 98% 이상의 바이러스 미검출 수준을 달성하고 꾸준히 유지됐으며 두 임상시험 모두 빅타비 단독요법군 중 내성으로 인한 치료 실패 사례는 관찰되지 않았다.
240주차까지 CD4+ 세포수 변화 중앙값은 Study 1489에서 313 cells/μL, Study 1490에서 331 cells/μL로 나타났다.1 CD4+ 세포수가 5년간 안정적으로 유지됐다.
두 임상시험에서 240주 동안 치료 관련 3-4 등급 이상의 이상반응을 보인 비율은 각각 1, 2명으로 낮았고 빅타비 단독요법군에서 치료 관련 이상반응으로 인해 치료를 중단한 비율은 1% 미만이었다.
길리어드 사이언스 코리아 이승우 대표는 "HIV 감염의 장기 관리의 중요성이 점차 부상하고 있는 가운데 초치료 5년 장기 데이터 허가사항 추가 소식을 전할 수 있어 기쁘다"며 "장기적인 바이러스 억제 효과와 안전성을 제공하고 내성 발생 걱정 없이 복용할 수 있는 혁신 약제를 개발·공급하기 위해 앞으로도 힘쓰겠다"고 말했다.