로그인
 로그인을 하시면 메디칼타임즈의
로그인을 하시면 메디칼타임즈의다양한 연관서비스를 이용하실 수 있습니다. 가입 시 등록한 정보를 입력해주세요.
 개인정보 보호를 위한 비밀번호 변경안내
주기적인 비밀번호 변경으로 개인정보를 지켜주세요.
개인정보 보호를 위한 비밀번호 변경안내
주기적인 비밀번호 변경으로 개인정보를 지켜주세요.안전한 개인정보 보호를 위해 3개월마다 비밀번호를 변경해주세요. ※ 비밀번호는 마이페이지에서도 변경 가능합니다.
30일간 보이지 않기
- 학술
- 학술대회
보리코나졸 부작용 이슈 재점화…허가 사항 변경되나
발행날짜: 2020-05-19 05:45:55
-
가
-
표피세포암 위험 증가 연구 보고…최대 3배 이상 위험
2012년, 2014년 이미 허가 변경…"해외 기관 사례 주시"
항진균제인 보리코나졸(Voriconazole)이 표피세포암 위험성을 높인다는 연구 결과가 나오면서 또 다시 부작용 이슈에 휘말릴 것으로 전망된다.
이미 국내에서도 2012년과 2014년에 부작용 이슈로 허가 사항이 변경된 적이 있다는 점에서 어떠한 영향을 미칠지에 관심이 모아지고 있는 것. 이에 대해 식품의약품안전처는 우선 해당 내용에 대한 해외 기관 사례를 주시하겠다는 입장이다.
보니코나졸 표피세포암 발생 위험 최대 3배 높여
미국 국립암연구소 모니카 애시(Monica E. D’Arcy) 박사가 이끄는 연구진은 항진균제 보리코나졸과 표피세포암 사이의 연관성에 대한 추적 관찰 연구를 진행하고 현지시각으로 17일 미국의사협회지(JAMA)에 그 결과를 게재했다.
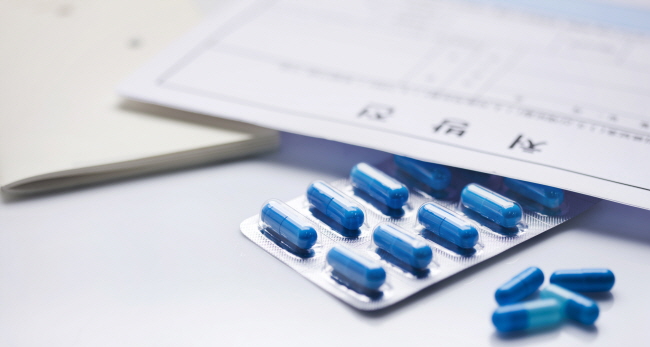
보리코나졸이 또 다시 표피세포암 등 부작용 이슈가 제기됐다.
연구진은 폐이식 등 이식 수술을 받는 환자들에게 아스페르길루스증 예방을 위해 항진균제 보리코나졸이 주로 처방되지만 이에 대한 부작용이 속속 보고되고 있다는 점에 주목했다.
이렇게 보리코나졸을 처방받은 환자 중에서 표피세포암 발생이 높다는 보고가 이어졌기 때문이다. 이에 따라 연구진은 2017년 1월부터 2016년 3월까지 9599명을 대상으로 보리콜라졸과 표피세포암 사이의 연관 관계를 조사했다.
평균 3년간의 추적 관찰 기간 동안 이들 환자들 중에는 총 1031명에게 표피세포암이 발병한 것으로 조사됐다. 통계적으로 분석하면 1만명 당 322명이다. 또한 347명은 여기서 유래한 기저세포암이 걸렸다. 이는 1만명 당 101명 꼴이다.
이렇듯 표피세포암이나 기저세포암이 발병한 환자들은 분명하게 보리코나졸과 연관성이 있었다. 특히 이러한 경향은 약물을 장기간 처방한 환자들에게서 분명한 경향이 드러났다.
1개월에서 3개월간 보리코나졸을 처방한 환자는 그렇지 않은 환자에 비해 표피세포암에 걸릴 확률이 1.09배 늘어났다.
하지만 4개월에서 7개월을 처방받은 환자는 대조군에 비해 1.42배 늘어났으며 8개월에서 15개월까지는 2.04배 위험이 증가한 것으로 분석됐다.
특히 15개월 이상 보리코나졸을 처방한 경우 표피세포암이 결릴 위험이 무려 3.05배나 높아지는 것으로 나타났다.
모니카 애시 박사는 "보리코나졸을 장기간 처방할 수록 표피세포암 위험이 크게 높아지는 것을 확인했다"며 "대체 약물로의 전환을 고려하거나 위험과 이익에 대한 고려가 필요하다"고 제언했다.
또 다시 대두된 부작용 이슈…처방, 허가 사항 변경될까
보리코나졸은 국내에서도 많은 양이 처방되는 다빈도 약물이라는 점에서 과연 이러한 부작용 이슈가 처방과 허가 사항에 영향을 줄지도 관심사다.
실제로 보리코나졸은 약물 농도의 개인차가 심한데다 특히 아시아인에게는 매우 느리게 대사되는 특징으로 인해 국내에서도 여러차례 부작용 이슈가 대두된바 있기 때문이다.
이로 인해 지난 2012년과 2014년 식품의약품안전처는 보리코나졸의 표준 용량이 한국 환자들에게 맞지 않는 점을 지적하며 허가 사항을 변경해 용량을 조절한 바 있다.
한국인의 경우 표준 용량인 400mg을 복용할 경우 정상대사자는 15337ng/ml·hr를 대사하지만 중간대사자는 29841ng/ml·hr, 대사저하자는 60749ng/ml·hr로 최대 4배까지 대사율에 차이를 보였기 때문이다.
이로 인해 국내에서도 간독성과 신부전 등의 부작용 이슈가 계속해서 학계에서 대두됐고 식약처는 국내 처방 용량을 4분의 1, 2분의 1로 줄일 것을 주문한 바 있다.
하지만 이제 막 부작용 이슈가 시작됐다는 점에서 아직까지는 곧바로 허가나 처방에 영향을 미치지는 않을 것으로 보인다. 다만 해외 사례를 주시하겠다는 것이 식약처의 입장이다.
식약처 관계자는 "관련 연구를 살펴봐야겠지만 아직까지 해외 허가 기관의 조치 등 허가 사항을 변경할 만한 사안은 파악되지 않았다"며 "지속적으로 해외 사례를 모니터링하며 상시 대응을 준비할 계획"이라고 말했다.
이미 국내에서도 2012년과 2014년에 부작용 이슈로 허가 사항이 변경된 적이 있다는 점에서 어떠한 영향을 미칠지에 관심이 모아지고 있는 것. 이에 대해 식품의약품안전처는 우선 해당 내용에 대한 해외 기관 사례를 주시하겠다는 입장이다.
보니코나졸 표피세포암 발생 위험 최대 3배 높여
미국 국립암연구소 모니카 애시(Monica E. D’Arcy) 박사가 이끄는 연구진은 항진균제 보리코나졸과 표피세포암 사이의 연관성에 대한 추적 관찰 연구를 진행하고 현지시각으로 17일 미국의사협회지(JAMA)에 그 결과를 게재했다.

이렇게 보리코나졸을 처방받은 환자 중에서 표피세포암 발생이 높다는 보고가 이어졌기 때문이다. 이에 따라 연구진은 2017년 1월부터 2016년 3월까지 9599명을 대상으로 보리콜라졸과 표피세포암 사이의 연관 관계를 조사했다.
평균 3년간의 추적 관찰 기간 동안 이들 환자들 중에는 총 1031명에게 표피세포암이 발병한 것으로 조사됐다. 통계적으로 분석하면 1만명 당 322명이다. 또한 347명은 여기서 유래한 기저세포암이 걸렸다. 이는 1만명 당 101명 꼴이다.
이렇듯 표피세포암이나 기저세포암이 발병한 환자들은 분명하게 보리코나졸과 연관성이 있었다. 특히 이러한 경향은 약물을 장기간 처방한 환자들에게서 분명한 경향이 드러났다.
1개월에서 3개월간 보리코나졸을 처방한 환자는 그렇지 않은 환자에 비해 표피세포암에 걸릴 확률이 1.09배 늘어났다.
하지만 4개월에서 7개월을 처방받은 환자는 대조군에 비해 1.42배 늘어났으며 8개월에서 15개월까지는 2.04배 위험이 증가한 것으로 분석됐다.
특히 15개월 이상 보리코나졸을 처방한 경우 표피세포암이 결릴 위험이 무려 3.05배나 높아지는 것으로 나타났다.
모니카 애시 박사는 "보리코나졸을 장기간 처방할 수록 표피세포암 위험이 크게 높아지는 것을 확인했다"며 "대체 약물로의 전환을 고려하거나 위험과 이익에 대한 고려가 필요하다"고 제언했다.
또 다시 대두된 부작용 이슈…처방, 허가 사항 변경될까
보리코나졸은 국내에서도 많은 양이 처방되는 다빈도 약물이라는 점에서 과연 이러한 부작용 이슈가 처방과 허가 사항에 영향을 줄지도 관심사다.
실제로 보리코나졸은 약물 농도의 개인차가 심한데다 특히 아시아인에게는 매우 느리게 대사되는 특징으로 인해 국내에서도 여러차례 부작용 이슈가 대두된바 있기 때문이다.
이로 인해 지난 2012년과 2014년 식품의약품안전처는 보리코나졸의 표준 용량이 한국 환자들에게 맞지 않는 점을 지적하며 허가 사항을 변경해 용량을 조절한 바 있다.
한국인의 경우 표준 용량인 400mg을 복용할 경우 정상대사자는 15337ng/ml·hr를 대사하지만 중간대사자는 29841ng/ml·hr, 대사저하자는 60749ng/ml·hr로 최대 4배까지 대사율에 차이를 보였기 때문이다.
이로 인해 국내에서도 간독성과 신부전 등의 부작용 이슈가 계속해서 학계에서 대두됐고 식약처는 국내 처방 용량을 4분의 1, 2분의 1로 줄일 것을 주문한 바 있다.
하지만 이제 막 부작용 이슈가 시작됐다는 점에서 아직까지는 곧바로 허가나 처방에 영향을 미치지는 않을 것으로 보인다. 다만 해외 사례를 주시하겠다는 것이 식약처의 입장이다.
식약처 관계자는 "관련 연구를 살펴봐야겠지만 아직까지 해외 허가 기관의 조치 등 허가 사항을 변경할 만한 사안은 파악되지 않았다"며 "지속적으로 해외 사례를 모니터링하며 상시 대응을 준비할 계획"이라고 말했다.

관련기사
- AIDS 치료제 '에파비렌즈' 뇌병증 등 신경독성 주의보 2020-02-11 11:42:39
- 차세대 P-CAB 보노프라잔, 혈액·림프계 이상반응 신설 2020-01-10 11:41:46
- 등 떠밀린 식약처, 원칙없는 특별 재평가 정당할까 2019-11-18 05:45:00
- 해외기관에 의존하는 식약처…허가부터 사후관리 '구멍' 2019-10-08 05:30:58
- 신약 안전성 보고서 허점 투성이...시정조치도 4% 수준 2019-10-07 10:50:02
학술 기사
- 세계 염증성 장질환의 날 "국내 환자 지속 증가세" 2020-05-18 11:19:54
- 술 마시는 사람은 갑상선암 적게 걸린다? 'NO' 2020-05-18 10:05:41
- 미리보는 ASCO...화두는 면역항암제 반응률 최강 조합 2020-05-18 05:45:57
- CAR-T 치료제 ‘예스카타’ 동반질환 있는 환자도 효과 2020-05-15 12:30:55
- 마이크로바이옴 치료제 상용화 임박…시장 진입 초읽기 2020-05-15 05:45:57
학술 기사
많이 읽은 뉴스
이메일 무단수집 거부
메디칼타임즈 홈페이지에 게시된 이메일 주소가 전자우편 수집 프로그램이나
그 밖의 기술적 방법을 이용하여 무단으로 수집되는 것을 거부하며,
이를 위반할 시에는 정보통신망법에 의해 형사 처벌될 수 있습니다.
그 밖의 기술적 방법을 이용하여 무단으로 수집되는 것을 거부하며,
이를 위반할 시에는 정보통신망법에 의해 형사 처벌될 수 있습니다.









- 최신순
- 추천순
댓글운영규칙ex) medi****** 아이디 앞 네자리 표기 이외 * 처리
댓글 삭제기준 다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입이 제한될 수 있습니다.
1. 저작권・인격권 등 타인의 권리를 침해하는 경우
2. 상용프로그램의 등록과 게재, 배포를 안내하는 게시물
3. 타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
4. 욕설 및 비방, 음란성 댓글