재허가 받은 '자이프렉사' 오리지널 경쟁력 이어나갈까
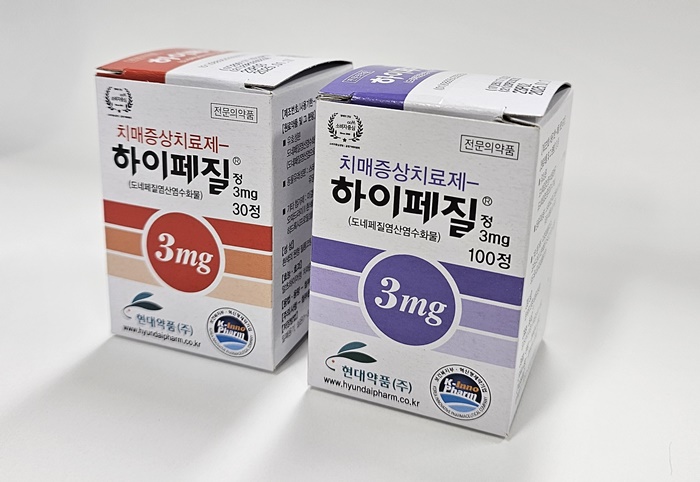
메디칼타임즈=문성호 기자올란자핀 성분 조울증 치료제 시장을 둘러싼 제약사 간 협력 관계가 다시금 주목을 받고 있다.해당 성분 오리지널 품목을 보유한 제약사들이 최근 임상현장에서 활용이 늘어나고 있는 항우울제 치료제 시장 수성을 놓고 협력을 이어가기 때문이다.3일 제약업계에 따르면, 최근 릴리는 식품의약품안전처로부터 '자이프렉사 자이디스(미세올란자핀)' 재허가를 받았다.올란자핀 성분 조울증 치료제 오리지널 품목인 자이프렉사 제품사진.릴리에 앞서 보령도 올란자핀 성분 오리지널 품목인 자이프렉사를 용량 마다 재허가를 식약처로부터 받은 바 있다.이 같은 릴리와 보령의 움직임이 주목받는 이유는 자이프렉사를 둘러싼 양사의 관계 때문이다. 여기서 자이프렉사는 1996년 출시된 이래 전 세계에서 가장 많이 처방된 조현병 치료제다. 조현병과 양극성장애에 쓰이는 약물로, 뇌속 도파민의 불균형을 조절하는 기전이다.의약품 시장조사기관 아이큐비아에 따르면 자이프렉사는 지난해 국내에서 153억원의 매출을 올렸다. 복제의약품(제네릭)이 출시한 상황에도 '올란자핀' 성분 시장에서 약 50%의 점유율을 차지하며 오리지널 품목의 지위를 유지하고 있다.이 가운데 보령은 2021년 7월 985억원 규모의 유상증자를 실시하면서 밝힌 LBA(Legacy Brands Acquisition) 전략의 일환으로 자이프렉사를 릴리로부터 인수했다.임상현장에서 장기간 쓰인 오리지널 품목의 국내 판권‧허가권을 인수, 강한 영업력을 앞세워 지위를 유지해나가겠다는 전략이다. 릴리로부터 항암제 '젬자(젬시타빈염산염)'의 국내 권리를 인수한 것도 같은 전략으로 해석된다.다만, 릴리는 당시 '자이프렉사자이디스'를 보령과의 계약 과정에서 남겨뒀다.제약업계 관계자는 "자이프렉사 자이디스를 릴리가 재허가 받으면서 보령이 보유한 자이프렉사까지 오리지널 품목 라인이 유지될 것"이라며 "보령이 자이프렉사 자이디스까지 국내 판매를 맡기 때문에 보령이 임상현장 지위가 그대로 유지되는 것"이라고 말했다.한편, 국내 임상현장에서 코로나19 대유행을 기점으로 조울증 환자가 늘어나면서 항우울제 시장은 날이 갈수록 커지고 있다.국내사들 대부분 특허가 만료된 주요 글로벌 제약사의 오리지널 항우울제 품목의 제네릭을 출시한 상태다. 최근에는 저용량 제품까지 출시, 조울증 뿐만 아니라 다양한 환자층에서의 쓰임새가 늘어나고 있다.익명을 요구한 서울의 A대학병원 정신건강의학과 교수는 "개인적인 의견이지만 이전과 다르게 최근 대학병원과 개원가에 방문하는 환자 특성이 크게 차이가 나지 않는다"며 "면담 위주로 하는 의원급 의료기관이 늘어나면서 약물 치료에 전향적인 형태로 진료 문화가 발전했다"고 설명했다.근는 "자이프렉사 뿐만 아니라 다양한 품목들이 항우울제 저용량 품목이 나오는데 주 치료 약물보다는 그에 동원되는 보조 약물로 승부하려는 것 같다. 소화기내과 등 다양한 진료과목에서 항우울제 활용도가 커지고 있다"며 "병원과 의원급 의료기관의 환자 특성의 차이가 희미해진 상황에서 부가 치료제로 활용도가 높아지고 있다"고 전했다.