인터뷰
"먹는 인슐린 앞세워 바이오기업 대열로 올라서야죠"
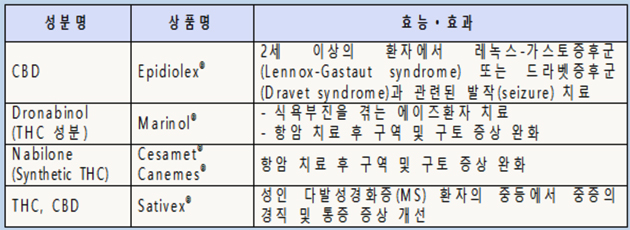
메디칼타임즈=황병우 기자"의료 사각지대라고 할 수는 없지만 경제적 여건 등을 이유로 소외된 환자들이 존재한다. 치료제 개발뿐만 아니라 다양한 치료제를 국내로 들여와 이러한 환자들의 빈자리를 채우는 빛과 같은 역할을 하고 싶다."제약바이오 산업이 미래 먹거리로 부상하면서 연구기술을 바탕으로 한 바이오벤처 기업의 창업부터 대기업의 진출까지 이어지며 점차 외연이 확장되고 있다.활발한 진출이 이뤄지고 있는 만큼 어떠한 방향성을 가지고 시장에 접근하느냐가 회사가 가진 경쟁력을 가늠하는 하나의 지표로 작용하고 있는 것도 현실.오대환 대표대형 선박의 특수 블록(콕스) 생산을 주력으로 해온 메디콕스(옛 중앙오션) 역시 제약바이오 분야를 기업의 미래로 점찍은 상황.메디콕스 오대환 대표는 의약품 유통 사업과 신약개발이라는 투트랙을 바탕으로 국내 제약바이오 시장의 문을 두드리고 있다는 점을 강조했다.메디콕스는 콕스(cox)라고 부르는 대형선박의 맨 하단에 곡선으로 된 선미와 선수부분을 현대중공업에서 공급해왔던 회사다.여기에 제약바이오 분야를 더해 메디콕스로 사명을 변경하면서 사업을 다각화 한 상태. 다르게 해석하면 기존 사업이 있는 만큼 제약바이오 분야 진출의 동력이 탄탄하다는 의미로도 바라볼 수 있다.오 대표는 "제약바이오 분야는 이미 다양한 기업이 진출한 미래 먹거리라는 점에서 국내사와 외자사 중간 지점의 바이오벤처 형태의 제약사를 그리고 있다"며 "자회사인 메콕스큐어메드에서 진행하는 신약개발과 라이센스인을 통한 기술이전, 의약품 유통까지 구상하고 있는 상태다"고 설명했다.현재 메디콕스가 가장 주목하는 분야는 경구용 인슐린 국내 유통과 관련된 부분이다.메디콕스는 오라메드파마슈티컬즈(이하 오라메드)가 개발 중인 제2형 당뇨병 경구용 인슐린 후보물질 ORMD-0801의 국내 독점 유통계약을 체결했다. 올해 말이나 내년 초 3상 탑라인 발표가 있을 것으로 전망되면서 실제 허가도 가시화 된 만큼 기대감도 높은 상태다.오 대표는 "경구용 인슐린은 매우 획기적인 아이템이지만 이미 많은 기업들이 성공하지 못한 만큼 충분히 기술적인 확인을 한 뒤에 계약을 체결했다"며 "이미 인슐린은 개발된 지 100년이 넘은 안전한 제품으로 유효성과 안전성에 대한 3상 결과가 긍정적으로 나올 것으로 바라본다"고 말했다.국내 인슐린 시장 규모는 약 3000억원에 달하는 파이를 가지고 있는데다 전 세계적으로 봐도 33조원 규모로 연 7%의 성장세를 보이고 있다.하지만 국내에서는 주사제에 대한 거부감으로 인해 상대적으로 다른 치료제 분야와 대비해 시장의 활성도가 떨어진 상태다. 즉, 경구용 인슐린이 허가를 받아 들어오게 된다면 국내 인슐린 시장을 확장시킬 수 있는 셈이다.오 대표는 "3상 결과를 바탕으로 미국에서 빠르면 2023년 하반기 보수적으로 잡아도 2024년 초에 신약허가가 날 것으로 전망한다"며 "국내의 경우 가교 임상의 변수가 있지만 현재로선 이르면 2024년 말 국내 출시가 가능할 것으로 기대한다"고 밝혔다.그는 이어 "보수적으로 국내 인슐린 시장이 4000억원 대로 봤을 때 허가를 받을 시 1500~2000억원 가량의 매출을 기대하고 있다"며 "추후 급여의 문제가 남아있지만 인슐린 특성상 상대적으로 영향은 덜할 것으로 보고, 마케팅 운영은 직접 하되 제약영업은 국내사와 진행하는 코웍 형태를 구상 중이다"고 언급했다.오대환 대표"제약분야 진출 신뢰 쌓기 위한 노력 이어갈 것"또한 메디콕스가 준비하고 있는 분야는 소아 뇌전증 치료물질 CBD(Epidyolex, 에피디올렉스, 성분명 칸나비디올) 오일 수입 유통이다.CBD오일 대마의 칸나비디올(CBD) 성분을 추출한 오일로, 국내에서는 2세 이상의 소아뇌전증인 '레녹스-가스토 증후군'과 '드라베 증후군' 환자에게 처방되고 있다.오 대표는 "해외에서 장기적인 처방을 통해 안정성이 있고 가격 경쟁력이 있는 치료제를 들여오기 위해 다각도로 노력하고 있는 중이다"며 "국내에는 긴급승인 받은 단일 제품 하나만 사용하고 있는 상황에서 환자들에게 가격 부담이 있는 만큼 접근성 측면에서 혜택을 줄 것으로 기대한다"고 강조했다.이밖에도 메디콕스는 노인질환이나 산부인과 질환에 화된 치료제를 통해 캐시카우를 확보하기 위한 협의 혹은 계획을 구상 중에 있는 상황이다.큰 틀에서 봤을 때 메디콕스의 사업 확장이라는 목표가 있지만 CBD 오일과 경구용 인슐린 모두 소아 환자 등 상대적으로 소외된 환자에게 치료제를 제공하는 역할이라는 점에서 기업의 색깔을 알 수 있는 부분이다.그는 "인슐린의 경우 주사제기 때문에 소아환자가 투여하는데 애로사항이 있고 CBD 오일 역시 의료용 대마와 관련해서 여전히 어려움이 많은 상황"이라며 "외자사가 치료제를 들여와도 약가 때문에 출시가 되지 못하는 제품이 많은데 이러한 부분에서 회사가 역할을 하길 바란다"고 말했다.끝으로 오 대표는 "메디콕스를 설립한 것은 좋은 약들을 국내 시장에 맞춰서 가져오고 신약개발에도 힘을 쏟기 위한 것"이라며 "아직 제약바이오분야에 진출한 기간이 짧은 만큼 신뢰를 쌓아가는 것이 어려운 일이지만 소외된 환자에게 희망이 되는 회사가 되기 위해 노력하겠다"고 덧붙였다.