신약시장 제3의 물결 유전자치료제, 현실 적용 과제는?
메디칼타임즈=원종혁 기자 'NGS(차세대염기서열분석) 검사'나 '유전자패널 검사'가 실제 진료현장에 접목되기 시작하면서, 원인을 알길이 없어 치료가 어려웠던 희귀질환자들까지도 관리의 가능성이 열리고 있다.
다만 증세를 줄이거나 질병자체를 완화시키려는 목적이 강했던 기존 화학합성의약품들이나 바이오 생물학적제제에 기대기에는 치료법의 한계가 분명했던 상황. 복잡한 사슬처럼 얽힌 유전자 돌연변이가 문제의 근원으로 지적되기 때문이다.
그래서 최근 의학계는, 이러한 환자들을 대상으로 유전자치료(gene therapy)나 유전자편집(gene editing) 등의 첨단 의료기술을 적극 활용한 유전자치료제를 그 해결책으로 주목하고 있다.
이미 2010년대 초반, 유전자치료 분야에 인프라를 구축하고 상용화를 위해 뛰어든 글로벌제약기업들은, 첨단 유전자치료제를 1900년대 등장한 소분자의약품(제1의 물결)과 1980년대 진입한 바이오생물학적치료제(제2의 물결)를 잇는 '제3의 혁신적 물결'로 인정하는 분위기다.
이러한 변화의 흐름은, 식품의약품안전처(처장 이의경) 주최로 지난 7일부터 9일까지 3일간 열린 '2020 글로벌바이오컨퍼런스(이하 GBC)' 자리에서도 뚜렷하게 포착됐다.
올해로 6회째를 맞은 이번 GBC는 '첨단 바이오, 사람 중심의 가치창조'를 주제로 18개국 61명(해외34명)의 국내외 바이오 분야 전문가들과 규제기관 관계자들이 참여해 코로나19 치료제 백신 개발동향을 비롯한 첨단 바이오의약품 개발현황에 대한 전문가 논의를 진행했다. 행사는 코로나19 대유행의 영향으로 전면 온라인으로 진행됐다.
이번 GBC에서는 특히, 지난 8월28일부로 시행된 '첨단 재생바이오법'으로 인해 높아진 첨단 바이오의약품에 대한 관심을 반영하듯 차세대 의학기술에 대한 화두가 중심에 올랐다. 이 자리에서는 최근, 유망 코로나19 백신 개발로 선두권에 이름을 올린 화이자제약의 유전자치료제 분야 투자 전망과 개발현황에 대한 상세 계획이 소개되며 주목을 받았다.
이와 관련해, 유전자치료제 분야 글로벌 리더인 화이자 글로벌 유전자치료사업부 로버트 조셉 스미스(Robert Joseph Smith) 수석 부사장과 희귀질환사업부 혈우병, 내분비, 유전성 대사질환 및 이식부문 글로벌 메디컬리드 이안 윈번(Ian Winburn) 부사장이 연자로 참여해 유전자치료로 변화하는 환자관리 패러다임과 생태계 변화는 이미 시작됐다고 분석했다.
유전자치료제 패러다임 "실질적 결과물 이끈 집중 투자"
일단 유전자치료는 환자와 보호자들은 물론 지역사회에 매우 큰 변화를 불러일으킬 수 있는 잠재력을 가지는 것으로 내다보고 있다. 기능적 완치를 통해 환자 삶의질과 생산성을 높일 수 있으며, 한 번의 치료로 장기간 질환에 대한 부담을 감소시킬 수 있을 것으로 기대되기 때문. 효과와 안전성이 입증되면, 중장기적인 측면에서 치료 효율성을 높이고 헬스케어산업의 재정건전화 역시 기대할 수 있는 이유에서다.
산업계 전문가들은 유전자치료제로 인한 치료 패러다임의 변화는 바이오산업 전반에 걸쳐 나타나고 있으며, 특히 희귀질환 영역에서 두드러지고 있다는 점을 지목했다.
로버트 수석부사장은 "화이자는 이미 유전자치료제 개발에 필요한 기술적인 플랫폼을 갖추고 있으며, 새로운 치료법의 불확실성에 대한 위험 역시 감수하며 세계적으로 비즈니스를 운영해오고 있다"고 강조하면서 "희귀혈액질환을 비롯한 내분비대사질환, 심혈관계질환, 신경계질환 영역으로의 확장과 새롭게 부상하고 있는 유전자치료 분야에 리더십 구축을 목표로 잡고 있다"고 설명했다.
실제 전세계 100개국 이상에서 1,000명 이상의 희귀질환 전담 인력들이 신규 치료제 개발에 돌입한 상황이며, 약 8억달러(약9,500억원) 이상을 투자해 미국노스캐롤라이나에 3개의 유전자치료제 전문 제조시설을 건설했다.
주목할 점은, 이같은 투자가 손에 잡히는 결과물을 만들고 있다는 대목이다. 2019년 기준 화이자 희귀질환사업부의 매출은 20억달러(약 2조3,750억원)를 넘어선 상황이다.
빨라진 기업인수합병 파트너십 "총322개 유전자 프로젝트"
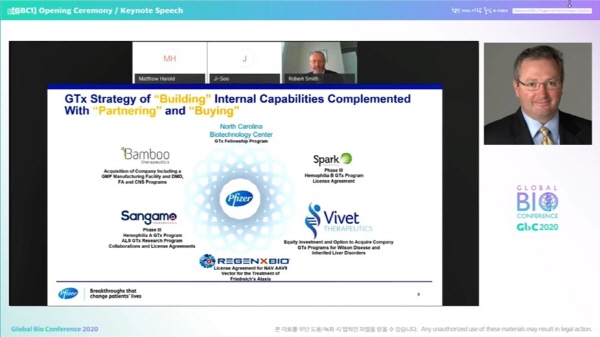
이러한 첨단 유전자치료제 개발에는 내부 개발역량을 적극 활용하는 것과 동시에, 다양한 외부 파트너십과 인수합병 전략도 주효한 개발전략으로 평가된다.
출처: 발표 내용 중 .
화이자가 진행해온 유전자치료제 관련 파트너십 및 인수합병 현황을 살펴보면, '오픈 이노베이션'이나 '오픈 콜라보레이션'의 성과도 확인해볼 수 있다.
세부적으로 스파크테라퓨틱스(Spark Therapeutics)와의 협업을 통해 혈우병B 유전자치료 프로그램의 3상임상을 진행중이며, 상가모테라퓨틱스(Sangamo Therapeutics)와 혈우병A 유전자치료 프로그램의 3상임상, 루게릭병이라고도 알려져 있는 근위축성축삭경화증(amyotrophic lateral sclerosis, ALS) 연구 프로그램 등을 함께 진행해오고 있다.
이밖에도 뱀부테라퓨틱스(Bamboo Therapeutics)를 인수해 듀시엔형 근이영양증(Duchenne muscular dystrophy, DMD), 프리드리히운동실조증(Friedreich's ataxia, FA), 중추신경계질환 등에 연구를 이어가고 있으며, 프랑스의 유전자치료제 전문 개발사인 비벳테라퓨틱스(Vivet Therapeutics)의 지분을 인수해 윌슨병(Wilson Disease) 및 유전성 간질환 치료제 개발에도 뛰어든 상황이다.
유전자치료 "바이오 생물학적제제 잇는 제3의 물결될 것"
유전자치료제의 가능성을 평가하는 질환영역도 광범위하다. 희귀질환 치료를 위해 신경계질환을 비롯한 혈액질환, 안과질환, 내분비대사질환, 심혈관계질환 등에서 총322개의 유전자치료제 개발프로그램을 운영하고 있는 것이다.
이 가운데 절반 이상인 66%가 생체내 아데노연관바이러스(in vivo AAV)를 활용한 접근방식을 취하고 있으며, 약 14%의 프로그램이 생체외(ex vivo) 방식을 채택했다. 유전자편집(gene editing) 프로그램은 전체 개발 프로젝트중 2%에 불과해 아직 큰 비중을 차지하고 있지는 않지만, 향후 혁신이 기대되는 분야인만큼 관련 연구도 준비중인 분위기다.
로버트 부사장은 발표를 통해 "화이자는 지난 2014년 유전자치료 분야에 본격적인 투자를 시작했다"면서 "유전자치료가 제약바이오산업에 있어 1900년대 질병의 증상을 완화하는 소분자의약품(제1의 물결), 1980년대 질병자체를 완화하는 바이오 생물학적치료제(제2의 물결)를 잇는 혁신적인 제3의 물결이 될 것으로 예상했기 때문"이라고 강조했다.
그러면서 "현재까지 알려져 있는 약 7,000여종의 희귀질환 가운데 약 80% 이상이 유전성인 것으로 알려져 있어 질병의 기저원인을 직접적으로 치료하는 새로운 개념의 유전자치료제는 치료의 패러다임을 근본적으로 바꾸게될 것"이라고 전망했다.
접근성 확보와 불확실성 과제 "가치평가 기준 재정립 필수"
유전자치료에는 크게 '유전자치료(gene therapy)' '유전자편집(gene editing)' '후생유전학(epigenetics)' 등 세가지 접근법으로 나뉜다. 다국적제약기업인 화이자는 개발현황을 통해 이같은 유전자치료 영역중 '생체내 재조합 아데노연관바이러스(in vivo rAAV)' 기반의 유전자치료에 집중하고 있다고 전했다.
출처: 발표 중 유전자치료제란 도표 일부.
'생체외방식(ex vivo)'은 환자 자신의 세포를 직접이용해 치료대상이 제한적인 반면, '생체내방식(in vivo)'은 특정 유전자를 바이러스벡터(viral vector)로 감싸 환자에게 주입하는 방식으로 유전자를 직접 전달하기 때문에 많은 환자를 동일한 방식으로 치료할 수 있기 때문이다.
재조합 아데노연관바이러스(rAAV)는 비병원성으로 알려진 병원체가 없고, 유전자를 캡슐화(incapsulation)할 수 있어 매우 효율적으로 표적조직에 유전자를 전달할 수 있다. 동일한 특정질환을 가진 환자들에 일괄적으로 적용하기 좋다는 장점을 가지는 것이다.
이안 부사장은 "유전자치료가 매우 큰 잠재력을 가지고 있는 것은 사실이지만, 치료제 개발에 성공하고 규제당국의 승인을 받더라도 원활한 치료를 위한 시스템구축, 적절한 접근성 확보, 불확실성에 대한 관리에 과제 역시 공존한다"고 말했다.
특히, 유전자치료제에 대한 적절한 접근성을 확보하기 위해서는 유전자치료제의 가치를 평가하는 새로운 시각과 접근이 필요하다고 강조했다. 희귀질환은 환자수가 매우 적어 표준치료(standard of care)를 수립하는 것이 어렵고, 질병의 완화효과를 측정하거나 표준화하기 어렵기 때문에 치료제의 비용효과성(cost effectiveness) 역시 기존 약제와 동일한 잣대로 평가하기란 쉽지 않기 때문이다.
따라서 환자 삶의질이 높아짐으로써 다시 사회로 복귀해 생산적인 활동에 참여하는 개선혜택 등 환자의 전 생애주기를 고려한 유전자치료의 가치를 평가해야 한다는 주장이 속속 나오는 이유다.
효과나 안전성 측면에서도 지속적인 장기 모니터링과 데이터 수집 관리가 중요한 분야이므로, 이를 위한 정부의 정책적인 지원은 물론 업계와의 논의 및 협업과정도 필수적으로 꼽았다.
끝으로 이안 부사장은 "유전자치료제가 직면하고 있는 다양한 문제들은 결국 불확실성에 기인하며 정책적인 접근을 통해 적극적으로 해소해야 한다"며 "유전자치료가 가진 임상적, 재정적 측면에서의 불확실성을 낮추려면 환자들에 장기간의 모니터링, 데이터 수집, 분석이 효율적으로 진행돼야 한다. 불확실성을 관리하기 위해 적극적인 투자는 물론 다양한 인센티브에 많은 고민을 진행해오고 있다"고 말했다.